продолжение
Серебряная вода
Для проведения электролиза следует приготовить соответствующую установку. Главная часть установки – серебряные электроды. Их можно отлить из ненужных серебряных изделий.
В том случае, если есть сомнения в подлинности серебряных предметов, можно провести несложный химический анализ. На поверхность серебряного изделия наносится капля раствора дихромата калия (К2Сr2О7), подкисленного серной кислотой. Оба реактива есть даже в школьной химической лаборатории, так же их используют при выделке меха. Приготовленный раствор быстро портится, поэтому анализ надо делать сразу, а по завершении его раствор утилизировать. Если содержание серебра в сплаве превышает 25 %, то в месте соприкосновения капли с изделием образуется ярко красный осадок дихромата серебра. Однако если достоверно известно, что содержание серебра в сплаве низкое, то использовать его не стоит, так как при одновременном присутствии в сплаве нескольких металлов, в раствор будет переходить преимущественно более активные металлы, входящие в состав сплава. Желательно использовать серебро не ниже 916 пробы, т.е. содержание серебра в таком сплаве составит 91.6 %. При желании, зная пробу серебра, можно внести соответствующие коррективы и формулу для расчета времени электролиза. Для этого рассчитанное время надо поделить на 1/1000 долю от значения пробы, в данном случае на 0.916.
Для
отливки электродов можно воспользоваться обыкновенным строительным кирпичом,
пропилив на его поверхности продольную канавку, длиной 70 –
При использовании электродов любого типа необходимо раз в 10 – 15 минут менять полюса источника питания на противоположные, во избежание появления на серебряных электродах нерастворимых пленок. При сильном загрязнении электродов их можно почистить мелким абразивом.
Для электролиза используется стеклянная банка, необходимого объема . Качество воды и правила использования полученного раствора оговаривались выше. Банку заполняют водой, до такого уровня, что бы она не касалась поверхности крышки, в противном случае она по капиллярам может просочится до места соединения электродов с проводом. Провода подключают к источнику питания через миллиамперметр, используя показания которого рассчитывают время электролиза и осуществляют процесс.
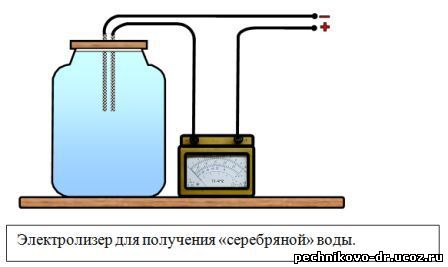
В качестве источника питания можно воспользоваться несколькими батарейками, соединенными последовательно, аккумуляторами на 6-12 вольт, или низковольтным источником питания постоянного тока из кабинета физики.
Эксперименты, с использованием серебряной воды можно провести такие:
- Исследование анитимикробных свойств серебряной воды.
Для этого эксперимента понадобятся растворы серебряной воды разной концентрации. Так как диапазон концентраций растворов, при которых серебряная вода проявляет свои свойства достаточно широк, то следует приготовить группу растворов, в которых концентрация ионов серебра между соседними растворами будет отличатся в 5, а то и в 10 раз. Так, например, можно приготовить растворы с концентрацией ионов серебра, образующей ряд значений в 0.01, 0.1, 1.0, 10 и 100 мг/л. Конечно же следует сделать и контроль, без ионов серебра. Растворы разливаются в химические стаканчики, объемом по 50-100 мл. На каждые 50 мл раствора добавляется по 5 мл. крепкого, профильтрованного через ткань бульона. Бульон нельзя солить, для того, чтобы не допустить выпадение в осадок хлорида серебра. Во избежании путаницы стаканчики маркируются. Стаканчики ставятся в теплое место для обеспечения быстрого развития микроорганизмов. Через каждые сутки в определенное время оценивается интенсивность запаха раствора и делаются соответствующие выводы.
- Сравнение антимикробных свойств серебряной воды, приготовленной путем электролиза и растворением нитрата серебра.
- Исследование влияния хлоридов на антимикробные свойства серебряной воды.